Principales estrategias de recuperación tras un ictus en 2026 para resultados duraderos
Las personas que sobreviven a un ictus y sus cuidadores se enfrentan a decisiones abrumadoras al elegir enfoques de rehabilitación en 2026. Con tecnologías innovadoras como interfaces cerebro-ordenador, sistemas robóticos y neurofeedback adaptativo entrando en la práctica clínica, comprender qué estrategias ofrecen resultados reales es crítico. Esta guía examina métodos basados en la evidencia que han demostrado mejorar la función motora y las actividades diarias, ayudándole a identificar las opciones más efectivas para una recuperación significativa.
Índice
- Criterios para seleccionar estrategias efectivas de recuperación tras un ictus en 2026
- Tecnologías de interfaz cerebro-ordenador (BCI) en la rehabilitación del ictus
- Terapia asistida por robots y control mioeléctrico para la recuperación del miembro superior
- Comparación de estrategias principales de recuperación: interfaces cerebro-ordenador, robótica y neurofeedback
- Explorar kits y herramientas eficaces para la rehabilitación del ictus
- ¿Cuáles son las estrategias de recuperación tras un ictus más efectivas en 2026?
Puntos clave
| Punto | Detalles |
|---|---|
| La intervención temprana importa | Las terapias iniciadas en las fases aguda o subaguda con más de 12 horas de dosis total muestran mejores resultados en comparación con el tratamiento retrasado. |
| La tecnología BCI mejora la recuperación | Las interfaces cerebro-ordenador ayudan a reconstruir vías neuronales y mejoran la función motora y las actividades diarias tanto en pacientes con ictus agudo como crónico. |
| Los sistemas robóticos potencian la función | La terapia asistida por robots mejora significativamente la función motora, la fuerza de agarre y la participación social cuando se combina con la rehabilitación convencional. |
| La retroalimentación adaptativa optimiza el entrenamiento | El control mioeléctrico con retroalimentación en RV ayuda a normalizar los patrones de activación muscular y acelera la recuperación del miembro superior en supervivientes de ictus. |
 Criterios para seleccionar estrategias efectivas de recuperación tras un ictus en 2026
Criterios para seleccionar estrategias efectivas de recuperación tras un ictus en 2026
Elegir el enfoque de rehabilitación adecuado requiere entender qué distingue a las intervenciones efectivas de las menos eficaces. La evidencia muestra claramente que tanto el momento de inicio como la dosis influyen en el éxito de la recuperación: las intervenciones iniciadas temprano y administradas de forma intensiva producen mejores resultados.
Al evaluar estrategias de recuperación, considere estos factores clave:
- Momento de la intervención: Empezar la terapia durante las fases aguda o subaguda suele dar mejores resultados que el tratamiento retrasado.
- Dosis total de terapia: Las investigaciones indican que superar las 12 horas de dosis total de terapia se asocia con ganancias funcionales significativas.
- Intensidad y duración: Las sesiones de mayor intensidad durante periodos adecuados inducen cambios de neuroplasticidad con más eficacia que esfuerzos esporádicos.
- Perfil de deterioro individual: Ajuste la complejidad y el tipo de intervención a sus déficits motores específicos y a la etapa de recuperación.
- Integración tecnológica: Combine herramientas emergentes con la rehabilitación convencional para una recuperación multimodal y completa.
Su etapa de recuperación importa considerablemente. Los pacientes en fase aguda pueden beneficiarse de terapia convencional intensiva combinada con aumentos tecnológicos. Los supervivientes en fase crónica con frecuencia obtienen ganancias con neurofeedback y enfoques BCI que atacan déficits persistentes. Entender en qué punto del proceso se encuentra ayuda a priorizar las intervenciones de forma adecuada.
Consejo profesional: Registre sus horas de terapia semanalmente para asegurarse de alcanzar el umbral basado en la evidencia de más de 12 horas de dosis total durante las ventanas tempranas críticas de recuperación. Pequeñas sesiones diarias se acumulan más rápido de lo que cree.
El marco de trabajo de las 7 recomendaciones esenciales de rehabilitación ofrece orientación adicional sobre cómo estructurar su programa de rehabilitación para máxima eficacia.
Tecnologías de interfaz cerebro-ordenador (BCI) en la rehabilitación del ictus
Las interfaces cerebro-ordenador suponen un avance para ayudar a los supervivientes de ictus a recuperar el control motor al traducir directamente las señales cerebrales en comandos de movimiento. Estos sistemas funcionan detectando la actividad neural asociada con la intención de movimiento y proporcionando retroalimentación en tiempo real que ayuda a reconstruir las vías neuronales dañadas.
La evidencia clínica demuestra que las intervenciones BCI benefician la función motora de las extremidades inferiores y las actividades de la vida diaria en pacientes con ictus en distintas fases de recuperación. La tecnología resulta particularmente valiosa porque involucra los mecanismos naturales de aprendizaje del cerebro, reforzando la conexión entre intención y acción.
La imaginación motora combinada con BCI (MI-BCI) muestra resultados especialmente prometedores. Cuando usted usa MI-BCI como terapia complementaria, mejora tanto las puntuaciones de función motora como las capacidades en las actividades diarias en comparación con la rehabilitación convencional sola. Este enfoque consiste en que usted ensaye mentalmente movimientos mientras el sistema BCI proporciona retroalimentación que confirma cuando su cerebro genera las señales motoras apropiadas.
“El neurofeedback no invasivo en circuito cerrado puede guiar la recuperación motora en pacientes post-ictus con deterioro motor crónico, produciendo mejoras clínicamente significativas.”
Ventajas clave de la tecnología BCI incluyen:
- Eficacia en fase crónica: Funciona incluso años después del ictus cuando la terapia tradicional se estanca.
- Reconstrucción de vías neuronales: Reconstruye activamente circuitos de control motor dañados mediante retroalimentación dirigida.
- Intensidad personalizada: Adapta la dificultad automáticamente al nivel de capacidad actual.
- Mejora del compromiso: Ofrece confirmación visual o sensorial inmediata de la actividad neural.
La naturaleza no invasiva de los sistemas BCI modernos los hace prácticos tanto para entornos clínicos como domésticos. El neurofeedback en circuito cerrado produce mejoras motoras medibles sin cirugía ni dispositivos implantados, reduciendo las barreras de acceso.
Aunque la evidencia es prometedora, la investigación actual sobre BCI incluye tamaños de muestra relativamente pequeños. Ensayos más amplios en curso en 2026 aspiran a establecer protocolos definitivos e identificar qué perfiles de pacientes se benefician más. Por ahora, combinar BCI con mejoras en la rehabilitación motora y con los mejores ejercicios de rehabilitación tras un ictus ofrece el enfoque más completo.
Considere explorar metaanálisis sobre rehabilitación con BCI para una comprensión técnica más profunda de los mecanismos y resultados.
Terapia asistida por robots y control mioeléctrico para la recuperación del miembro superior
Los sistemas exoesqueléticos robóticos transforman la rehabilitación del miembro superior al proporcionar asistencia de movimiento precisa y repetible que intensifica la terapia más allá de lo que las técnicas manuales logran por sí solas. Estos dispositivos soportan su brazo afectado mediante patrones de movimiento funcionales mientras miden métricas de rendimiento en tiempo real.
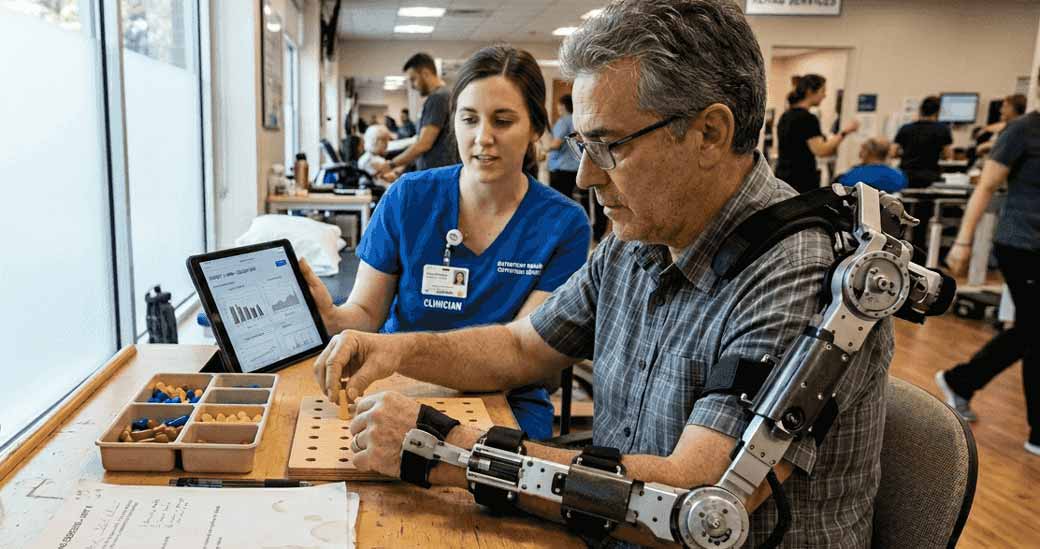
El sistema robótico ReHand demuestra la eficacia de estas tecnologías. Los estudios muestran que el robot ReHand mejora la recuperación del miembro superior en pacientes con ictus subagudo cuando se añade a los protocolos de terapia estándar. Su diseño portátil permite sesiones de práctica intensiva que agotaría a un terapeuta humano, ofreciendo un mayor número de repeticiones crítico para el aprendizaje motor.
El control mioeléctrico aporta otra dimensión potente a la terapia robótica. Este enfoque captura señales eléctricas residuales de sus músculos, incluso si son débiles, y las traduce en comandos de movimiento para dispositivos de asistencia o avatares virtuales. Combinado con retroalimentación visual adaptativa en entornos de RV, el control mioeléctrico con retroalimentación en RV mejora los patrones de activación muscular y la calidad del movimiento.
El componente de retroalimentación adaptativa resulta especialmente valioso porque ajusta automáticamente la ganancia visual según su rendimiento. Si genera señales débiles, el sistema amplifica la respuesta visual para mantener la motivación y el compromiso. A medida que su control mejora, la escala de retroalimentación cambia para desafiarle de forma adecuada.
Comparación de enfoques de terapia robótica
| Tipo de sistema | Mecanismo principal | Mejor para | Ventaja clave |
|---|---|---|---|
| Robots exoesqueléticos | Asistencia física al movimiento | Déficit severo, fase subaguda | Alto número de repeticiones, métricas objetivas |
| Control mioeléctrico | Amplificación de señales residuales | Déficit moderado, fase crónica | Activa las vías neuronales restantes |
| Sistemas integrados con RV | Retroalimentación visual adaptativa | Todos los niveles de gravedad | Aumenta la motivación y el compromiso |
| Robots de efector final | Entrenamiento orientado a tareas | Práctica con objetivos funcionales | Traduce directamente a actividades diarias |
Los metaanálisis confirman que la terapia asistida por robots mejora significativamente múltiples dominios de resultado, incluyendo función motora, fuerza de agarre, actividades de la vida diaria y participación social. Estos beneficios integrales justifican la inversión en equipos para muchos programas de rehabilitación.
Consejo profesional: Al usar sistemas robóticos, centrese en la calidad de la intención de movimiento más que en completar repeticiones mecánicas. Los beneficios de la neuroplasticidad provienen de implicar activamente su cerebro en el movimiento, no de permitir pasivamente que el robot mueva su brazo.
Integrar la terapia robótica con ejercicios convencionales maximiza los resultados. Mientras que los robots sobresalen en la práctica repetitiva y en la medición objetiva, complementan en lugar de sustituir la terapia manual, el entrenamiento funcional y la rehabilitación domiciliaria en los programas de recuperación tras un ictus.
El panorama de la tecnología en la recuperación neuro sigue evolucionando rápidamente, y 2026 trae opciones más asequibles y portátiles adecuadas para uso doméstico junto con sistemas de grado clínico.
Consulte los protocolos detallados del ensayo del sistema robótico ReHand para entender cómo estas intervenciones se integran en programas de rehabilitación completos.
Comparación de estrategias principales de recuperación: interfaces cerebro-ordenador, robótica y neurofeedback
Comprender cómo se comparan las principales tecnologías de rehabilitación le ayuda a tomar decisiones informadas sobre qué enfoques se adaptan a sus necesidades y circunstancias de recuperación. Cada método aborda distintos aspectos de la recuperación motora mediante mecanismos diferentes.
Matriz comparativa de estrategias
| Estrategia | Objetivo terapéutico | Ventajas principales | Limitaciones | Calidad de la evidencia |
|---|---|---|---|---|
| Sistemas BCI | Reconstrucción de vías neuronales | Efectivo en fase crónica, no invasivo | Resultados variables, estudios con muestras pequeñas | Moderada, en mejora |
| Terapia robótica | Entrenamiento físico del movimiento | Alta repetición, datos objetivos, eficacia probada | Acceso al equipo, coste | Fuerte, metaanálisis disponibles |
| Neurofeedback adaptativo | Modulación de la actividad cerebral | Dificultad personalizada, retroalimentación en tiempo real | Tecnología emergente, datos a largo plazo limitados | Prometedora, necesita ensayos más amplios |
| Control mioeléctrico | Amplificación de señales residuales | Utiliza la capacidad neural existente, motivador | Requiere algo de actividad muscular | Moderada, evidencia creciente |
 Una revisión exhaustiva de los métodos de rehabilitación con BCI subraya que, aunque cada enfoque muestra potencial, existen lagunas importantes en la evidencia sobre protocolos óptimos, criterios de selección de pacientes e implementación en el hogar y la comunidad.
Una revisión exhaustiva de los métodos de rehabilitación con BCI subraya que, aunque cada enfoque muestra potencial, existen lagunas importantes en la evidencia sobre protocolos óptimos, criterios de selección de pacientes e implementación en el hogar y la comunidad.
La tecnología BCI destaca cuando la terapia convencional llega a un estancamiento, especialmente en supervivientes de ictus en fase crónica. La capacidad de trabajar directamente con señales neuronales en lugar de requerir movimiento físico la hace valiosa para déficits severos. Sin embargo, la variabilidad de respuesta entre individuos implica que algunos pacientes mejoran de forma espectacular mientras otros obtienen ganancias moderadas.
La terapia asistida por robots ofrece actualmente la base de evidencia más sólida en múltiples medidas de resultado. La tecnología beneficia particularmente a pacientes subagudos y a aquellos con déficits severos que necesitan práctica intensiva y repetitiva. El acceso sigue siendo una barrera, ya que muchos sistemas requieren entornos clínicos, aunque las opciones portátiles que emergen en 2026 abordan esta limitación.
Los enfoques de neurofeedback adaptativo como el Magnetic NeuroRing representan fronteras emocionantes en la tecnología de la rehabilitación. Estos sistemas modulan los patrones de actividad cerebral en tiempo real, acelerando potencialmente el aprendizaje motor. Los resultados iniciales son prometedores, pero continúan los estudios de validación más amplios a lo largo de 2026.
Combinar múltiples enfoques suele producir resultados superiores respecto a protocolos de un solo método. Por ejemplo, emparejar la retroalimentación BCI con la asistencia robótica aprovecha tanto el entrenamiento neural como la práctica física. De igual modo, la terapia convencional proporciona el contexto funcional que hace que las intervenciones tecnológicas se traduzcan en capacidad en la vida real.
Las lagunas de investigación que debe conocer incluyen datos limitados sobre resultados a largo plazo más allá de los periodos iniciales de intervención, tamaños de muestra pequeños en muchos estudios e investigación insuficiente sobre qué características del paciente predicen la mejor respuesta a tecnologías específicas. Los principios de la neuroplasticidad en la recuperación tras el ictus que sustentan estos métodos están bien establecidos, pero los protocolos óptimos siguen evolucionando.
Al seleccionar estrategias, priorice enfoques basados en la evidencia adecuados para su fase de recuperación y la gravedad de su deterioro. Los supervivientes en fases tempranas suelen beneficiarse más de la terapia convencional intensiva aumentada selectivamente con tecnología. Los individuos en fase crónica a menudo encuentran mayor valor en BCI y enfoques de neurofeedback que atacan déficits persistentes resistentes a métodos tradicionales.
Revise la revisión sobre estrategias BCI para obtener detalles técnicos sobre consideraciones de implementación y enfoques de medición de resultados en las distintas categorías tecnológicas.
Explorar kits y herramientas eficaces para la rehabilitación del ictus
Traducir los hallazgos de la investigación en recuperación práctica requiere herramientas accesibles que incorporen terapia basada en la evidencia en su rutina diaria. La tecnología de rehabilitación ya no requiere exclusivamente entornos clínicos: los sistemas domésticos sofisticados ahora ofrecen intervenciones de nivel profesional.
Tisele Rehab ofrece kits de rehabilitación para la recuperación tras un ictus diseñados alrededor de los mismos principios de neuroplasticidad que impulsan las tecnologías clínicas. Productos como FitMi, el sistema de neurorrehabilitación doméstica, proporcionan ejercicios interactivos tipo juego que aumentan la dosis de terapia entre las sesiones formales. El dispositivo de rehabilitación manual MusicGlove utiliza actividades motivadoras para ofrecer la práctica repetitiva esencial para el aprendizaje motor, facilitando alcanzar el umbral de más de 12 horas de terapia asociado a mejores resultados. Estas herramientas complementan estrategias avanzadas como BCI y terapia robótica al asegurar un progreso constante durante su recuperación, no solo en las citas programadas.
¿Cuáles son las estrategias de recuperación tras un ictus más efectivas en 2026?
¿Qué estrategias de recuperación tras un ictus muestran la evidencia más sólida en 2026?
Las interfaces cerebro-ordenador, la terapia asistida por robots y el neurofeedback adaptativo demuestran beneficios significativos en múltiples ensayos clínicos. La terapia convencional sigue siendo la base, con la tecnología aumentando y no reemplazando los enfoques tradicionales para obtener resultados óptimos.
¿Cuándo debo comenzar la rehabilitación intensiva tras un ictus?
Comience tan pronto como sea médicamente seguro, idealmente durante las fases aguda o subaguda. La intervención temprana con una dosis adecuada (más de 12 horas en total) produce de forma constante ganancias funcionales superiores frente al tratamiento retrasado.
¿Pueden los supervivientes de ictus crónico beneficiarse de las nuevas tecnologías de rehabilitación?
Absolutamente. Los sistemas BCI y el neurofeedback adaptativo muestran particular promesa para la recuperación en fase crónica cuando la terapia tradicional alcanza un estancamiento. Estas tecnologías activan mecanismos de plasticidad neural que siguen activos años después del ictus.
¿Necesito un entorno clínico para una rehabilitación eficaz tras un ictus?
Aunque los programas clínicos ofrecen estructura y experiencia importantes, las herramientas de terapia domiciliaria aumentan significativamente el tiempo total de práctica. Combinar sesiones profesionales con práctica doméstica constante usando sistemas basados en la evidencia maximiza el potencial de recuperación.
¿Cómo mejoran los sistemas robóticos los resultados de la recuperación tras un ictus?
La terapia robótica ofrece práctica de alta repetición con asistencia precisa al movimiento y seguimiento objetivo del rendimiento. Los estudios confirman mejoras en función motora, fuerza de agarre, actividades diarias y participación social cuando se añade a la rehabilitación estándar.
¿Qué papel juega la dosis de terapia en la recuperación tras un ictus?
La dosis de terapia impacta directamente en los resultados; la investigación muestra que más de 12 horas totales es un umbral relevante. Mayor intensidad y duración impulsan cambios de neuroplasticidad más fuertes, por lo que la práctica diaria consistente es esencial para lograr ganancias funcionales significativas.
Recomendado
38
Inspírese con una de las historias de los convalecientes del accidente cerebrovascular
Ludificación en fisioterapia, muy buena terapia.
Tuve un infarto hace 9 años y ya estaba usando muchas terapias diferentes. Me gusta mucho ludificación, que me está dando
MusicGlove.
La estoy usando desde solo un mes, pero ya veo progreso en mis posibilidades. Me lo motiva mucho, es increíble.
En general – el MusicGlove me encanta.
Tomasz S. (04.03.2020)









